Hi, Sobat Zenius! Kali ini gue mau sharing materi larutan basa kelas 11. Yukkkkk… Sobat Zenius kelas 11, merapat!
Elo pernah memiliki riwayat penyakit maag gak? Maag merupakan kondisi di mana tubuh memproduksi asam lambung berlebih. Untuk mengobati maag tersebut, elo bisa menggunakan obat maag yang merupakan contoh basa yang bermanfaat untuk menetralisir asam lambung adalah antasida yang ampuh menetralkan kadar asam di dalam lambung.
Sifat dari obat tersebut adalah basa. Dengan begitu, basa dalam antasida akan bereaksi dengan HCl atau asam lambung dan membuatnya netral. Sehingga, maag elo bisa teratasi.
Lalu, basa itu sebenarnya apa sih? Kok bisa digunakan sebagai obat maag, cara kerjanya bagaimana? Contoh basa lainnya apa aja? Apa aja ciri ciri larutan basa? Daripada semakin penasaran, langsung aja deh scroll ke bawah untuk mendapatkan jawabannya!
Daftar Isi
Apa Itu Larutan Basa?
Basa merupakan larutan. Sobat Zenius taukan kalau pH dari asam itu <7, nah sedangkan yang merupakan larutan basa memiliki pH > 7.
Larutan yang bersifat basa adalah licin jika dilarutkan dalam air dan pada dasarnya zat yang bersifat basa memiliki rasa pahit! Eh tapi elo tidak boleh mencicipi suatu larutan untuk mengetahui apakah larutan tersebut termasuk dalam basa atau bukan.
Bisa aja kan larutan yang elo cicipi ternyata bersifat korosif, tentu itu termasuk hal yang membahayakan. Untuk mengujinya, elo bisa menggunakan kertas lakmus dan fenolftalein.

Teori Basa Menurut Arrhenius
Seorang ilmuwan asal Swedia bernama Svante Arrhenius (1859-1897), menjelaskan bahwa basa zat yang melepaskan ion OH- dalam air.
Jika ada yang bertanya, NaOH asam atau basa? Jawabannya basa. Dan di bawah ini dengan basa Arrhenius digambarkan dalam M(OH)x yang diuraikan di dalam air sbb:
M(OH)x → Mx+ + xOH–
Contohnya:
Natrium hidroksida = NaOH → Na+ + OH–
Kalium hidroksida = KOH → K+ + OH–
Kalsium hidroksida = Ca(OH)2 → Ca2+ + 2OH-
Dan menurut teori arrhenius NH4OH merupakan senyawa basa karena dapat melepaskan ion OH- dalam larutannya.
NH4OH akan terurai sesuai dengan persamaan reaksi berikut:
NH4OH ⇌ NH4+ + OH-
Ciri-ciri Larutan Basa
Elo udah baca tentang larutan asam belum? Larutan basa memiliki sifat yang sangat berlawanan dengan larutan asam lho. Ciri-ciri larutan basa antara lain, sbb:
- Larutan basa menyumbangkan pasangan elektron atau menyumbangkan ion hidroksida (OH-).
- Sama seperti larutan asam, larutan basa juga termasuk elektrolit. Tingkat kekuatannya tergantung dari banyaknya ion yang dihasilkan dalam air. Sama seperti larutan asam, basa juga ada yang kuat dan lemah.
- Salah satu ciri suatu larutan bersifat basa yaitu memiliki rasa pahit dan licin saat dilarutkan dalam air. Contohnya sabun.
- Basa dapat mengubah warna indikator kertas lakmus merah menjadi biru.
- Basa dapat mengubah warna fenolftalein menjadi merah muda.
- Basa tidak bisa bereaksi dengan logam.
- Basa bisa bereaksi dengan asam untuk menjadi garam.
Perlu juga elo ingat bahwa meskipun basa bisa diuji dengan menggunakan indera perasa, yaitu rasa pahit. Tapi, elo tidak boleh asal mencicipi suatu larutan. Hal itu karena larutan basa bisa bersifat korosif dan berbahaya untuk elo.
Kekuatan Basa
Sebelumnya udah gue bahas juga tentang kekuatan asam. Hampir sama dengan kekuatan asam, bahwa kekuatan basa juga ditentukan oleh jumlah ion OH- dan derajat ionisasi.
Basa yang dilarutkan dalam air akan mengalami reaksi peruraian menjadi ion. Dari situlah bisa ditentukan apakah larutan tersebut termasuk dalam basa kuat atau lemah. Selain itu, kekuatan basa juga bisa ditentukan oleh tetapan kesetimbangannya, yaitu tetapan ionisasi basa (Kb).
Reaksi kesetimbangan larutan basa bisa dituliskan seperti ini:
LOH (aq) ⇌ L+ (aq) + OH- (aq)
Tetapan ionisasi basa (Kb) bisa dirumuskan sbb:
Kb = [L+][OH-] / [LOH]
Basa Kuat
Basa kuat adalah larutan yang menghasilkan banyak ion dan terurai secara sempurna saat dilarutkan dalam air. Karena terionisasi sempurna, sehingga derajat ionisasinya (α=1). Contohnya adalah NaOH, KOH, LiOH, dan Ba(OH)2.
Berikut ini merupakan rumus ionisasi basa kuat:
[OH-] = x . [M(OH)x]
atau,
[OH-] = valensi basa . M
Basa Lemah
Apakah NH4OH basa kuat atau lemah? Jawabannya adalah basa lemah. Basa lemah adalah larutan yang menghasilkan sedikit ion dan sedikit terurai saat dilarutkan dalam air. Derajat ionisasi (0<α<1) Contoh basa lemah selain NH4OH adalah NaHCO3, Al(OH)3, AgOH.
Berikut ini merupakan rumus ionisasi asam kuat:
[OH-] = akar dari Kb.[M(OH)]
atau,
[OH-] =[M(OH)].α
Contoh Soal dan Pembahasan
Setelah kamu memahami tentang penjelasan materi larutan basa, sekarang kita masuk ke contoh soal dan pembahasan. Yuk, coba dan perhatikan soal beserta pembahasannya berikut ini!
Soal:
Tentukan konsentrasi ion OH- dalam masing-masing larutan berikut.
- KOH 0,004 M
- Al(OH)3 0,1 M jika Kb = 2,5 x 10^-6
- NH4OH 0,01 M jika terion sebanyak 5%
Pembahasan:
Larutan KOH merupakan basa kuat, sedangkan Al(OH)3 dan NH4OH termasuk basa lemah.
———-
Demikian pembahasan mengenai larutan basa. Nah, sekarang elo udah paham ‘kan sama larutan basa dan rumus ionisasinya?
Agar lebih jelas lagi, elo bisa banget belajar materi larutan basa di video pembahasan materi Zenius atau untuk mempelajari materi Kimia lain bisa langsung klik banner di bawah. Semoga penjelasan di atas dapat bermanfaat untuk elo, ya. Have a nice day!
———-
Baca Juga Artikel Kimia Lainnya
Larutan Elektrolit dan Non Elektrolit
Originally Published: February 25, 2021
Updated By: Arieni Mayesha









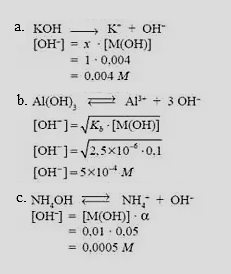

Leave a Comment