Halo Sobat Zenius! Elo masih ingat gak apa sih yang dimaksud dengan larutan? Gimana ya proses pelarutan itu? Oke, di artikel kali ini, kita akan bahas larutan, proses pengenceran larutan, dan pencampuran larutan.
Sebelum itu, gue mau menyamakan persepsi dulu nih sama elo mengenai larutan. Coba elo perhatikan ilustrasi di bawah ini.
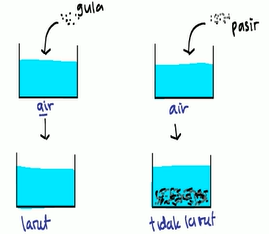
Ketika elo memasukkan gula ke dalam air, maka gula akan larut dalam air dan menjadi campuran homogen. Sedangkan, ketika elo memasukkan pasir ke dalam air, maka pasir gak bisa larut dan akan menjadi campuran heterogen.
Nah, untuk kasus yang pertamaーgula dan airーbisa kita sebut sebagai larutan dan yang keduaーpasir dan airーdisebut dengan suspensi. Artinya:
“Larutan merupakan campuran homogen yang terdiri dari zat terlarut dan pelarut.”
Baca Juga: Pengertian Larutan dan Klasifikasinya – Materi Kimia Kelas 11
Daftar Isi
Apa Itu Pengenceran Larutan?
Elo pernah dong bikin sirup, tapi masih kemanisan? Apa yang kemudian dilakukan, apakah elo akan menambah air? Nah, yang elo lakukan itu adalah salah satu praktik pengenceran larutan.
Setelah melakukan pengenceran dengan cara menambah air, maka rasa manisnya pun akan berkurang, iya gak? Rasa manis ini berkaitan dengan konsentrasi. Ketika rasa manisnya berkurang, maka konsentrasi gula dalam larutan tersebut berkurang. Kok bisa sih konsentrasinya berkurang setelah ditambahkan air?
Baca Juga: Tata Nama Senyawa Kimia, Ionik dan Kovalen – Materi Kimia Kelas 10
Rumus Pengenceran Larutan
Jadi gini, suatu larutan itu kan ada partikel zat terlarut dan pelarutnya. Ketika larutan tersebut ditambahkan air, maka volume larutan akan bertambah. Tapi, partikel-partikel di dalamnya tetap, dengan kata lain gak bertambah dan gak berkurang. Biar gak bingung, coba lo perhatikan ilustrasi berikut ini.
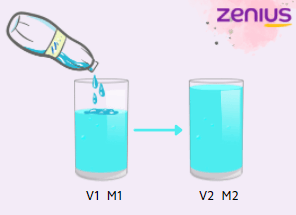
Di dalam suatu larutan, kita bisa mengetahui volume, molaritas, dan molnya. Karena proses pengenceran gak mengubah jumlah partikel zat terlarut, maka nilai molnya sama, yaitu n1=n2. Bisa kita tulis rumus pengencerannya
n1 = n2
V1.M1 = V2.M2
Keterangan:
n: mol
V1: volume larutan awal
M1: molaritas awal
V2: volume larutan setelah ditambah air
M2: molaritas larutan setelah ditambah air
Cara menghitung molaritas (M), yaitu:
Pencampuran Larutan
Oke, kita udah tahu nih apa dan gimana proses pengenceran larutan berlangsung. Lalu, gimana cara menentukan konsentrasi suatu larutan kalau ada larutan yang sejenis, tapi beda konsentrasi dicampurkan?
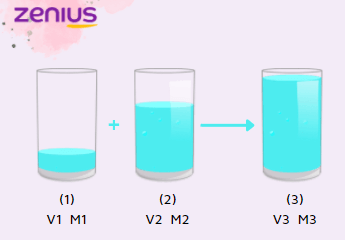
Ketika ada suatu larutan 1 dicampurkan dengan larutan 2 dengan konsentrasi yang berbeda, maka akan menghasilkan larutan total dari keduanya. Partikel di dalamnya tetap, yang berubah adalah konsentrasinya, sehingga bisa kita tuliskan rumus pencampuran larutan sebagai berikut:
n3 = n1 + n2
V3.M3 = V1.M1 + V2.M2
Baca Juga: Cara Menentukan Bilangan Oksidasi – Materi Kimia Kelas 10
Contoh Soal Pengenceran Larutan dan Pencampuran
Setelah elo memahami materi di atas, kita langsung masuk ke praktik perhitungannya, yuk! Contoh soal dan pembahasan mengenai pengenceran larutan dan pencampuran di bawah ini bisa elo jadikan sebagai referensi.
Contoh Soal 1
Sebanyak 20 ml larutan gula dengan konsentrasi 0,2 M ditambahkan air sebanyak 180 ml. Berapakah konsentrasi larutan gula sekarang?
a. 0,2 M
b. 2 M
c. 0,1 M
d. 0,01 M
e. 0,02 M
Jawab: e. 0,02 M.
Pembahasan: Rumus pengenceran adalah V1.M1 = V2.M2. Maka, konsentrasi larutan gula yang baru adalah 20(0,2) = 200.M2. Sehingga, M2 = 4/200 = 0,02 M.
Contoh Soal 2
Dua garam NaCl dicampurkan, jika larutan pertama memiliki konsentrasi 0,1 M dan larutan kedua memiliki konsentrasi 0,05 M. Maka, berapakah konsentrasi akhirnya jika kedua volume larutan sama besar?
a. 0,1 M
b. 0,015 M
c. 0,15 M
d. 0,07 M
e. 0,75 M
Jawab: d. 0,075 M.
Pembahasan: Gunakan rumus pencampuran di atas, sehingga kita peroleh uraian jawabannya sebagai berikut.
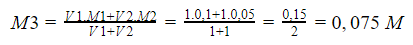
*****
Gimana nih, sampai sini udah paham kan tentang pengenceran larutan dan pencampurannya? Buat elo yang lebih menyukai belajar dengan nonton video, elo bisa mengakses materi ini di video belajar Zenius dengan cara klik gambar di bawah ini menggunakan akun yang sudah elo daftarkan di website dan aplikasi Zenius sebelumnya, ya!








Leave a Comment