Apa yang terlintas di benak Sobat Zenius saat mendengar kata atom? Kacang atom? Atau mungkin bom atom? Nah, di kelas 10 pada mata pelajaran Kimia, belajar materi struktur atom.
Struktur atom kelas 10 ini akan membahas secara lengkap, termasuk penjelasan mengenai partikel dasar atom, nomor atom dan nomor massa, hingga contoh atom di kehidupan sehari-hari.
Kalau elo punya suatu barang, contohnya kapur. Pernah gak sih elo kepikiran kalau kapur tersebut elo patahin, dipatahin terus sampe bagian terkecil dan gak bisa dipatahin lagi. Kira-kira bagian terkecil dari kapur atau benda tersebut akan disebut apa ya?
Nah, bagian terkecil dan tidak bisa terbagi lagi dari suatu benda inilah yang disebut dengan atom. Namun, setiap bagian kecil sekalipun tetap memiliki sifat yang sama.
Kenapa bisa dibilang sifatnya sama? Karena ketika elo mematahkan kapur menjadi 2, maka akan menjadi 2 kapur, di mana keduanya memiliki sifat dan partikel dasar yang sama bukan?
Partikel dasar atom itulah yang dinamakan struktur atom.
Dalam artikel ini gue akan bahas mengenai materi struktur atom, yang artinya kita bakal bahas struktur dasar dari bagian terkecil yang nggak bisa dilihat strukturnya dengan mata telanjang.
Selain itu, dalam artikel ini juga akan membahas mengenai nomor atom dan nomor massa, isotop, isobar, isoton, dan juga struktur atom dan konfigurasi elektron.
Daftar Isi
Dasar Teori Struktur Atom
Sebelum gue membahas mengenai materi struktur atom lebih jauh, gue akan memperkenalkan elo dengan dasar teori struktur atom.
Teori atom pertama kali dikemukakan oleh John Dalton (1803). Dalam teori ini atom dideskripsikan sebagai bagian terkecil yang tidak dapat diurai atau dibagi lagi.
John Dalton mengilustrasikan atom sebagai bola pejal yang sangat kecil dan bersifat identik sehingga setiap unsur memiliki atom yang berbeda juga.
Oleh karena itu struktur atom bisa didefinisikan secara sederhana sebagai susunan partikel dasar atom. Sebagai partikel penyusun sebuah materi, atom ikut menentukan sifat materi tersebut.
Sampai saat ini, tidak ada teori atau model yang mutlak dari sebuah atom, dan teori mengenai atom masih terus mengalami perbaikan, pengembangan, dan penyempurnaan.
Oh iya, sebelum kelupaan. Gue mau kasih info kalau materi struktur atom kelas 10 ini adalah salah satu materi yang sering muncul di UTBK lho.
Berarti elo harus menguasai materi Kimia yang satu ini supaya bisa menaklukan UTBK. Dan bukan cuman satu materi aja, Zenius juga punya daftar materi yang sering muncul di UTBK mulai dari berbagai mata pelajaran lengkap dengan contoh soal dan pembahasannya.
Buat elo para pejuang UTBK tahun ini, kalo mau tau rangkuman materi SBMPTN lengkap dengan pembahasannya, langsung klik gambar di bawah ya:
Partikel Dasar Struktur Atom
Meskipun dideskripsikan sebagai bagian terkecil yang tidak dapat diurai dan dibagi lagi ternyata atom disusun oleh beberapa partikel sub-atomik.
Partikel subatomik sebagai penyusun dasar dalam atom terdiri dari proton, elektron, dan neutron. Ketiga partikel dasar penyusun atom ini mempunyai perbedaan.
Suatu partikel dalam inti atom yang bermuatan positif disebut dengan proton. Sedangkan, elektron atom bermuatan negatif dan dalam sebuah atom neutron bersifat netral atau atom tidak bermuatan.
Supaya lebih jelas dalam memahaminya, di bawah ini ada tabel partikel-partikel atom:
| Jenis Partikel | Penemu/Tahun | Massa | Muatan | Lambang | Lokasi dalam atom |
| Proton | Goldstein 1886 | 1 | +1 | Inti atom | |
| Elektron | JJ Thompson 1897 | 0 | -1 | Di Luar inti atom | |
| Neutron | J. Chadwick 1932 | 1 | 0 | Inti atom |
Pada umumnya, atom terdiri dari ruang hampa yang didalamnya terdapat inti di mana massa dan muatan positifnya (+) berada di inti atom dan dikelilingi oleh elektron-elektron yang bermuatan negatif (-).
Sedangkan untuk inti atom terdiri dari proton dan neutron. Jumlah proton didalam inti atom inilah yang nantinya menentukan muatan inti atom, dan massa inti atom ditentukan oleh banyaknya jumlah proton dan neutron.
Elektron
Diketahui bahwa penemu dari elektron adalah JJ Thomson melalui percobaan sinar katode, sedangkan untuk muatan elektron sendiri ditemukan oleh Robert Millikan, melalui percobaan tetesan halus minyak.
Berdasarkan hasil percobaan Thomson dan Millikan, didapatkan muatan elektron -1 dan massa elektron sama dengan 0, sehingga elektron dilambangkan .
Proton
Untuk proton, ditemukan oleh Eugene Goldstein melalui percobaan sinar katode yang telah dimodifikasi.
Setelah melakukan percobaan pada berbagai gas, ditemukanlah bahwa gas hidrogen menghasilkan sinar bermuatan positif paling kecil baik massanya maupun muatan muatannya, sehingga partikel ini disebut proton.
Di mana proton memiliki muatan +1, dan massanya sama dengan 1 sma (satuan muatan atom).
Neutron
Penemu neutron adalah James Chadwick melalui percobaannya menembaki atom berilium dengan sinar alpha (𝛼).
Dari percobaan tersebut didapatkan bahwa partikel yang menimbulkan radiasi berdaya tembus tinggi memiliki sifat netral, atau bisa dikatakan tidak bermuatan, serta memiliki massa yang hampir sama dengan proton yaitu 1.
Oleh karena itu, dalam sebuah atom neutron bersifat netral karena partikel ini muatannya sama dengan 0 (nol).
Nomor Atom dan Nomor Massa
Partikel subatomik sebagai penyusun dasar dalam atom terdiri dari proton, elektron, neutron dengan kombinasi tertentu akan membentuk menjadi suatu unsur sebagai berikut:
A = Nomor Massa
Z = Nomor Atom
X = Lambang Unsur
Nomor atom (Z)
Nomor atom (Z) merupakan jumlah proton (muatan positif) atau jumah elektron dalam atom. Oleh karena atom bersifat netral maka jumlah proton = jumlah elektronnya.
Sehingga nomor atom juga menunjukkan jumlah elektronnya, dan nantinya merupakan hal yang menentukan sifat suatu unsur.
Nomor Massa (A)
Nomor massa (A) merupakan jumlah proton dan neutron. Nomor massa atau massa atom suatu unsur menyatakan banyaknya proton dan neutron yang menyusun inti atom suatu unsur.
Nomor Massa (A) = Jumlah Proton + Jumlah Neutron.
Lambang Unsur (X)
Lambang unsur (X) merupakan susunan suatu unsur netral, contohnya Oksigen lambang unsurnya (O).
Dari penjelasan gue di atas, bisa disimpulkan kalo nomor massa atau massa atom suatu unsur menyatakan banyaknya proton dan neutron.
Sedangkan nomor atom menyatakan banyaknya jumlah proton. Tapi saat suatu unsur netral maka nomor atomnya sama dengan elektron.
Isotop, Isobar, dan Isoton
Setelah memahami partikel sub-atomik sebagai penyusun dasar dalam atom yang terdiri dari proton, elektron, neutron serta penulisan dan lambang dari nomor atom dan nomor massa, ternyata ada juga unsur yang memiliki nomor atom yang berbeda meskipun memiliki nomor massa yang sama dan sebaliknya.
Oleh karena itu ada istilah isotop, isobar, dan isoton. Berikut ini adalah pengertian dan contohnya.
Susunan Elektron dalam Atom

Struktur atom dan konfigurasi elektron tidak dapat dipisahkan karena elektron yang selalu bergerak mengelilingi inti atom memiliki berbagai lapisan kulit atom pada tingkatan energi tertentu.
Nah, di bagian ini gue akan membahas materi struktur atom yang berhubungan dengan elektron atau partikel sub-atomik atom yang bersifat negatif.
Konfigurasi Elektron
Konfigurasi elektron merupakan penyusunan atau lapisan elektron berdasarkan tingkat energinya dalam suatu atom, di mana atom memiliki lapisan paling dekat dengan inti sampai yang terluar secara berurutan dari K, L, M, N, O, P, Q, dan seterusnya.
Di mana jumlah elektron maksimum pada suatu lapisan kulit memenuhi rumus , di mana n= nomor kulit, dan jumlah maksimum elektron pada kulit terluar adalah 8.
Contoh,
Lapisan kulit K (n=1) maksimum elektronnya= elektron
Lapisan kulit L (n=2) maksimum elektronnya= elektron
Lapisan kulit M (n=3) maksimum elektronnya= elektron
Dan seterusnya.
Contoh Soal
Tentukan konfigurasi elektron dari unsur Klorin (Cl)!
Jawaban:
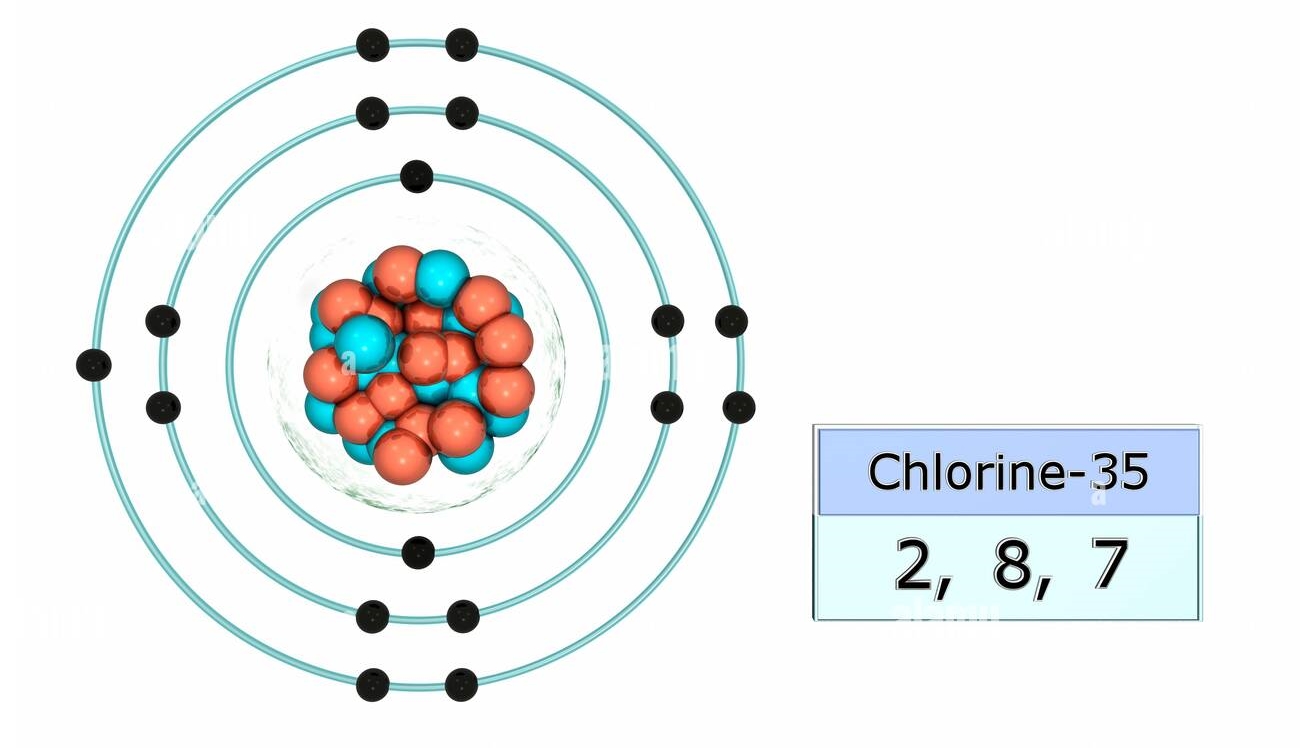
Nomor atom (Z) dari Cl= 17, maka
(Cl) = 2. 8. 7
Elektron Valensi
Berhubungan dengan konfigurasi elektron, elektron valensi merupakan jumlah elektron pada kulit terluar atom suatu unsur yang digunakan untuk membentuk ikatan kimia.
Oleh karena itu, susunan elektron valensi suatu unsur sangat mempengaruhi atau merupakan penentu sifat-sifat kimia suatu atom.
Unsur-unsur yang m
Contoh Soal
Tentukan elektron valensi dari Natrium (Na)!
Jawaban:
Nomor atom (Z) Natrium (Na) adalah 11, maka
(Na) = 2. 8. 1
Sehingga
Jumlah kulit Na = 3
Kulit terluar Na = M
Elektron valensi = 1
Nah, itu dia penjelasan gue mengenai materi struktur atom kelas 10. Kira-kira bagaimana Sobat Zenius? Sudah memahami partikel dasar struktur atom serta struktur atom dan konfigurasi elektron?
Selain belajar dari artikel ini, Sobat Zenius juga bisa banget, nih, belajar tentang struktur atom melalui video pembahasan dari tutor Zenius.
Cara aksesnya juga gampang, lho! Elo tinggal klik banner di bawah ini, ya! Lalu, ketikkan materi yang ingin elo pelajari di kolom pencarian.
Anyway, nggak cuma Kimia kalau elo juga pengen belajar mata pelajaran lainnya dengan paket komplet ditemani tutor asik, Sobat Zenius bisa berlangganan paket belajar yang udah kita sesuaikan dengan kebutuhan elo. Yuk intip paketnya!

Baca Juga Artikel Lainnya!
Larutan Elektrolit dan Non Elektrolit
Originally published: January 12, 2021
Updated by: Maulana Adieb dan Sabrina Mulia Rhamadanty











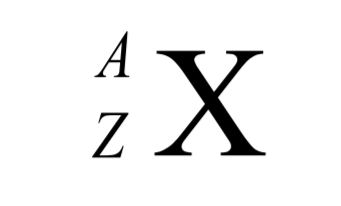

Leave a Comment